Rétinol
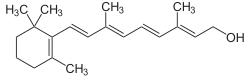
| Formule structurelle | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||
| Général | ||||||||||
| Nom commun | Vitamine A 1 | |||||||||
| Autres noms |
|
|||||||||
| Formule moléculaire | C 20 H 30 O | |||||||||
| Numero CAS | 68-26-8 | |||||||||
| code ATC | ||||||||||
| Brève description | solide jaune | |||||||||
| Occurrence | z. B. dans le poisson, le foie, le jaune d'œuf, le lait | |||||||||
| physiologie | ||||||||||
| fonction | Partie du pigment visuel, facteur de croissance, impliquée dans la formation de testostérone | |||||||||
| Besoin quotidien | 0,8-1,0 mg | |||||||||
| Conséquences en cas de carence | y compris la perte de cheveux, les troubles visuels (par exemple la cécité nocturne), l' atrophie des muqueuses et des glandes salivaires | |||||||||
| Surdosage | 7,5 mg | |||||||||
| Propriétés | ||||||||||
| Masse molaire | 286,46 g mol -1 | |||||||||
| État physique | fixé | |||||||||
| Point de fusion |
61-63°C |
|||||||||
| point d'ébullition |
120-125°C (0.67Pa) |
|||||||||
| solubilité |
|
|||||||||
| consignes de sécurité | ||||||||||
| ||||||||||
| Données toxicologiques | ||||||||||
| Dans la mesure du possible et d'usage, les unités SI sont utilisées. Sauf indication contraire, les données fournies s'appliquent à des conditions standard . | ||||||||||
Le rétinol , également vitamine A 1 ou axérophtol , est une vitamine essentielle liposoluble . Chimiquement parlant, le rétinol appartient aux diterpénoïdes et est un alcool primaire monohydrique . Le cycle de six atomes de carbone qu'il contient est appelé cycle β- ionone , et la molécule possède également un certain nombre de doubles liaisons conjuguées qui sont cruciales pour sa participation au processus visuel.
Souvent, le rétinol est également dans de nombreux manuels scolaires, la simplification, la vitamine A assimilée. Mais on entend par vitamine A plutôt un groupe de substances de -jononderivaten qui ont le même spectre d'activité biologique que le tout-trans-rétinol, à l'exclusion des pro-vitamines A .
histoire
Le rétinol a été découvert en 1913 par Elmer McCollum et Marguerite Davis (1887-1967). Ils l'ont décrit comme une vitamine liposoluble et son importance en tant que facteur antixérophtalmique. Ce n'est que 20 ans plus tard que la production pure de rétinol à partir d' huile de foie de morue a été réalisée par Paul Karrer .
La première synthèse totale de rétinol a été réalisée en 1947 par les chimistes néerlandais Jozef Ferdinand Arens (1914-2001) et David Adriaan van Dorp (1915-1995) par réduction progressive de la trétinoïne . Cette synthèse a été nommée d'après eux la synthèse d'Arens-van Dorp .
Ester de rétinyle
Les esters de rétinyle sont des conjugués de rétinol avec des acides gras . Les acides gras saturés acide palmitique et acide stéarique sont principalement utilisés pour la conjugaison, et en plus petites quantités les acides gras insaturés acide oléique , linoléique et linolénique .
Occurrence et besoin
Les animaux et les humains sont incapables de synthétiser la vitamine A de novo . La demande est satisfaite par l'alimentation. Alors que les carnivores absorbent la vitamine A principalement sous forme d'esters de rétinyle ou de rétinol, les herbivores utilisent les caroténoïdes comme source. Les principales sources alimentaires naturelles d'esters de rétinyle et de rétinol sont le foie , les huiles de foie de poisson ( huile de foie de morue ), les jaunes d'œufs ainsi que le lait et les produits laitiers , le foie en contenant de loin les plus grandes quantités.
Les humains peuvent utiliser le rétinol et les esters de rétinol, ainsi que la provitamine A pour répondre à leurs besoins en vitamine A . Comme la provitamine ne peut pas être utilisée de manière égale (absorption, conversion), son besoin est plus élevé.
De la Société allemande pour la nutrition (DGE) la nécessité pour les adultes avec
- 0,8… 1 mg de vitamine A ou de rétinol par jour
spécifié. 1 mg correspond à un équivalent rétinol de 1 mg. Avec le bêta-carotène, la quantité pour un équivalent de rétinol est de 6 mg, avec les autres provitamines A-caroténoïdes de 12 mg. 1,1 mg est recommandé pour les femmes enceintes et 1,5 mg pour les femmes qui allaitent, selon la quantité de lait.
Selon les études, la consommation de grandes quantités de rétinol ou de vitamine A, comme cela peut être le cas après un repas de foie ou une supplémentation surdosée, est suspectée d'avoir un effet tératogène.
Le chat a également besoin de rétinol ou de vitamine A 1 , mais a une position particulière car, contrairement à presque tous les autres animaux, il ne convertit pas le β-carotène en rétinol et ne peut donc naturellement obtenir suffisamment de vitamine A qu'en consommant du foie. Les croquettes sont donc souvent enrichies en lutéine issue de l' extrait de fleur de souci , que le chat peut transformer en rétinol.
Ingestion, stockage et mobilisation
Les esters de rétinyle sont la principale forme de vitamine A présente dans les aliments, mais ne peuvent pas être ingérés directement à partir des aliments. Tout d'abord, ils doivent être hydrolysés en rétinol dans la lumière intestinale . Une fois le rétinol absorbé dans les entérocytes, il est ré-estérifié avec des acides gras à longue chaîne .
Chez les mammifères, environ 50 à 80 pour cent de toute la vitamine A, constituée d'esters de rétinyle et de rétinol, se trouve dans le foie. Les cellules Ito dans le foie stockent environ 90 à 95 pour cent de cela. La quasi-totalité de la vitamine A (98%) dans les cellules Ito est sous forme d'ester et est emballée dans des gouttelettes de graisse. L'hydrolyse est donc également une condition préalable à la libération de la vitamine A par le foie. Celle-ci s'effectue sous l'action d'une enzyme (rétinyl ester hydrolase).
métabolisme
Le métabolisme de la vitamine A est principalement contrôlé par les RBP ( protéines liant le rétinol ). Ce n'est qu'avec leur aide que l'organisme peut utiliser la vitamine A, ce qui signifie qu'une carence en ces protéines peut entraîner des symptômes similaires à ceux de la carence en vitamine A ( hypovitaminose ) elle-même.
Si l'excès de rétinol ne peut pas être lié par les RBP, des symptômes d'empoisonnement apparaissent. Ils jouent donc également un rôle déterminant dans l'hypervitaminose A. Comme ils ont un doigt de zinc , l'oligo-élément zinc est important pour l'ensemble de l'équilibre en vitamine A - à la fois en cas de sous-approvisionnement et de surapprovisionnement.
Réactions
La biosynthèse des composés actifs de vitamine A est basée sur un ester de rétinyle (généralement du palmitate de vitamine A ) :
Le rétinol est le composant de base des rétinoïdes . L'oxydation de l'alcool conduit au rétinal , qui peut être encore oxydé en acide rétinoïque ( trétinoïne ).
synthèse
Une étape clé dans la production à grande échelle de vitamine A est la réaction de Wittig . Georg Wittig a reçu le prix Nobel de chimie en 1979 pour cette réaction largement applicable .
Dans la première partie de la synthèse, un sel en C 15 est produit à partir du déhydrolinalol . Celui - ci réagit par le biais de la réaction de Wittig avec un C 5 acétate, qui est produite à partir de dimethoxyacetone , pour former retinylacetate . Celui-ci peut être converti en rétinol en plusieurs étapes supplémentaires.
1 RE ( équivalent rétinol ) = 1 microgramme de rétinol = 6 microgrammes de β-carotène
Preuve individuelle
- ↑ a b c d Inscription sur le rétinol dans la base de données des substances GESTIS de l' IFA , consultée le 13 avril 2020. (JavaScript requis)
- ↑ a b Fiche technique Rétinol synthétique, ≥ 95% (HPLC), cristallin de Sigma-Aldrich , consulté le 24 novembre 2014 ( PDF ).
- ↑ Hanck, Kuenzle, Rehm: vitamine A . Blackwell Wissensch., Berlin, 1991 ISBN 978-3-8263-2879-4 .
- ^ McCollum & Davis (1913) : La nécessité de certains lipides pendant la croissance. Dans : J. Biol. Chem. Vol. 15, pages 167-175.
- ↑ Jozef Ferdinand Arens, David Adriaan van Dorp : Synthèse des aldéhydes de vitamine A. Dans : Nature . 1947, 160, page 189, doi : 10.1038 / 160189a0 .
- ↑ a b Thomas Arnhold : 1.4.1 Sources de vitamine A Dans : Études sur le métabolisme de la vitamine A/des rétinoïdes au regard d'une évaluation des risques de leurs effets tératogènes chez l'homme ; pages 6-7 ; Thèse; Braunschweig, 7 mars 2000. Texte intégral
- ↑ https://www.dge.de/wissenschaft/referenzwerte/vitamin-ab-carotin/ Vitamine A AJR recommandée de la DGE, consulté le 26 octobre 2018
- ↑ https://publikationsserver.tu-braunschweig.de/receive/dbbs_mods_00001088 Thomas Arnhold : Études sur le métabolisme de la vitamine A/des rétinoïdes au regard d'une évaluation des risques de leurs effets tératogènes chez l'homme ; Thèse Braunschweig 7 mars 2000; Page 179 et suivantes
- ↑ James G Morris : "Les besoins nutritionnels idiosyncratiques des chats semblent être des adaptations évolutives induites par l'alimentation" . Nutrition Research Reviews (2002), 15 : 153-168 Cambridge University Press
- ↑ Thomas Arnhold : 1.4.2 Absorption et métabolisme dans le tractus intestinal In : Études sur le métabolisme de la vitamine A/des rétinoïdes au regard d'une évaluation des risques de leurs effets tératogènes chez l'homme ; pages 7-8 ; Thèse; Braunschweig, 7 mars 2000. Texte intégral
- ^ Rune Blomhoff: Vitamine A dans la santé et la maladie , CRC Press 1994; P. 9. ISBN 9780824791209 .
- ↑ Thomas Arnhold : 1.4.4 Mobilisation à partir du foie et absorption dans les cellules extrahépatiques Dans : Études sur le métabolisme de la vitamine A/des rétinoïdes au regard d'une évaluation des risques de leurs effets tératogènes chez l'homme ; p. 7-8; Thèse; Braunschweig, 7 mars 2000. Texte intégral
- ↑ Thomas Arnhold : 1.2.3 Structure des rétinoïdes naturels et synthétiques In : Études sur le métabolisme de la vitamine A/des rétinoïdes au regard d'une évaluation des risques de leurs effets tératogènes chez l'homme ; p. 3; Thèse; Braunschweig, 7 mars 2000. Texte intégral

