Cétones
| Cétones |
|---|

|
| R 1 et R 2 sont des radicaux organiques (alkyle, aryle ou similaire). Le groupe carbonyle est marqué en bleu . |
Les cétones sont des composés chimiques qui contiennent un groupe carbonyle non terminal (> C = O) en tant que groupe fonctionnel . Un groupe cétone [C – C (O) –C] contient trois atomes de carbone. Toutes les cétones contiennent au moins trois atomes de carbone. Contrairement aux aldéhydes , ici le carbone carbonyle est lié à des atomes de carbone dans les deux sens. Les cétones peuvent être considérées comme des produits d'oxydation d' alcools secondaires . Les cétones qui peuvent être dérivées des alcanes sont également appelées alcanones . En conséquence, les cétones attribuables aux alcènes et aux alcynes sont appelées alcénones (voir énones ) ou alcynones . La cétone la plus simple est l' acétone . Une simple cétone aromatique est la benzophénone (diphényl cétone ). Une cétone mixte est l' acétophénone (méthyl phényl cétone ). Physiologiquement, certaines cétones sont produites sous forme de produits métaboliques dans le foie.
nomenclature
Après IUPAC - nomenclature obtenir les cétones le suffixe -on, le groupe carbonyle à condition que le groupe contenu dans la molécule avec la plus haute priorité soit. Ainsi, la cétone dérivée du propane est appelée propanone (CH 3 –CO – CH 3 , nom usuel : acétone ). Dans le cas des cétones à plus de trois atomes de carbone, le groupe carbonyle est situé dans la chaîne principale et reçoit le plus petit nombre possible ; cela peut être soit devant le nom, soit, dans le cas de molécules plus complexes, directement dans devant la terminaison -on. Par exemple : CH 3 -CH 2 -CH 2 -CO-CH 3 signifie 2-pentanone ou pentan-2-one. Si le groupe carbonyle n'a pas la priorité la plus élevée, le préfixe oxo est utilisé. Par exemple, CH 3 -CO-CH 2 -CHO 3-oxobutanal est appelé.
Cependant, les cétones ont très souvent des noms qui consistent en la désignation des radicaux alkyles suivis de la terminaison -cétone ( nomenclature radical-fonctionnelle ). Ainsi la butanone est aussi appelée méthyl éthyl cétone (MEK). Si l'un des substituants est un groupe phényle , la terminaison -phénon est courante, comme c'est le cas avec l' acétophénone par exemple .
Propriétés
Les cétones de faible poids moléculaire sont des liquides incolores, facilement mobiles et, en raison de la polarité du groupe carbonyle, sont solubles dans l'eau. Les cétones à faible poids moléculaire se caractérisent par une odeur fruitée généralement agréable . Les cétones de poids moléculaire supérieur sont des substances solides.
En raison de l' effet + I des substituants alkyle sur l'atome de carbone carbonyle, les cétones sont moins réactives que les aldéhydes et n'ont pas tendance à se polymériser . Contrairement aux aldéhydes, il n'y a pas de réaction avec les cétones dans le test de Fehling , car le groupe cétone ne peut pas être davantage oxydé tout en conservant la structure carbonée.
Fabrication
- Les cétones peuvent être produites en oxydant des alcools secondaires .
- Une autre méthode de production est l' ozonolyse des alcènes.
- La méthode de fabrication la plus importante pour les cétones aromatiques est l' acylation de Friedel-Crafts .
- Selon la synthèse des cétones par Gilman et van Ess , la cétone analogue est obtenue à partir d'un acide carboxylique (R 1 +1) et d'un composé lithium alkyl (R 2 ) par hydrolyse
- Une autre méthode de fabrication est la réaction des amides de Weinreb avec des composés d'alkyllithium et un traitement aqueux-acide ultérieur.
- La distillation dite des sels de chaux est une synthèse désormais historique , dans laquelle les sels de calcium des acides carboxyliques sont chauffés à sec et la cétone libérée sous forme gazeuse est recondensée (par exemple pour produire de l' acétone à partir d' acétate de calcium ).
- L'acétone est obtenue comme sous- produit dans la synthèse industrielle du phénol par le procédé à l'hydroperoxyde de cumène (procédé Hock).
- Ajout d'eau aux alcynes.
Réactions
Comme les aldéhydes , les cétones entrent dans des réactions d' addition et de condensation .
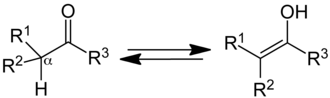
Les cétones (R 1 , R 2 , R 3 = radical organyle ) sont en équilibre avec leur forme tautomère , les énols ( tautomérie céto-énolique ), si un atome d'hydrogène est lié à l'atome de carbone :
Pour se protéger des réactions indésirables, les cétones sont converties avec des diols en acétals complets (voir groupe de protection ) :
Lorsque l'acétal complet est mis à réagir avec de l'eau, la cétone est à nouveau formée sous catalyse acide , c'est-à-dire H. le groupe protecteur est séparé.
Contrairement aux aldéhydes, les cétones ne peuvent être attaquées par oxydation que dans des conditions de réaction drastiques . Dans le processus, une liaison entre le carbone carbonyle et un carbone voisin est divisée. Les fragments moléculaires résultants sont des acides carboxyliques .
Représentants importants des cétones
utilisation
- Acétone : solvants , détergents
- Cyclohexanone : Fabrication de Perlon
- Cétone de framboise : aromatiser les aliments (odeur de framboise )
Spectroscopie des cétones
Dans les spectres IR des cétones et des aldéhydes , la bande caractéristique de la vibration d'étirement C = O se situe dans la plage de 1690 à 1750 cm -1 .
Voir également
Littérature
- K. Peter C. Vollhardt, Neil E. Schore : Chimie organique. 4e édition. Wiley-VCH, Weinheim 2005, ISBN 3-527-31380-X .
liens web
Preuve individuelle
- ↑ Joachim Buddrus : Fundamentals of Organic Chemistry , Walter de Gruyter Verlag, Berlin, 4e édition, 2011, p. 479, ISBN 978-3-11-024894-4 .