Groupe butyle
Le groupe butyle est un groupement d'atomes en chimie organique . Il appartient aux groupes alkyle et est formellement dérivé de la structure du butane par abstraction d'un hydrogène . Il a donc pour formule empirique C 4 H 9 . Le groupe butyle peut se présenter sous quatre formes isomères : en tant que n- butyle, iso- butyle (également « isobutyle »), sec- butyle et tert- butyle. Alors que dans le cas du groupe n- butyle et isobutyle , le reste est sur un primaire Si l'atome de carbone est lié, il est lié à un secondaire dans le cas du groupe sec- butyle et à un tertiaire dans le cas du groupe tert- butyle .
Propriétés
Propriétés stériques
Avec une ramification croissante, la demande stérique des groupes butyle augmente. Les groupes tert- butyle sont des résidus stériquement exigeants, ils peuvent être utilisés pour stabiliser des composés chimiques , car l'attaque peut être considérablement évitée en les remplissant. Cette gêne a également un effet sur la cinétique de réaction , qui peut être à la fois accélérée et ralentie en conséquence. Si des réactions qui nécessitent l'attaque d'un réactif à proximité du groupe tert-butyle ont lieu, ces réactions se déroulent généralement beaucoup plus lentement, car l'attaque est empêchée par le résidu de remplissage d'espace. A l'inverse, la conformation d' une molécule peut également être figée par le radical tert-butyle dans une position favorable à la cinétique de réaction et accélère ainsi la réaction. Le groupe tert-butyle agit ici comme un point d' ancrage .
Groupes d'ancrage
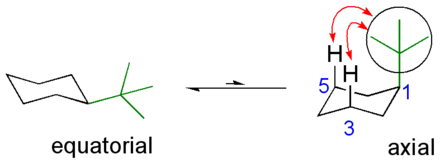
Les groupes isobutyle et tert-butyle peuvent être utilisés comme groupes d'ancrage. Cela signifie qu'ils entravent le changement de conformation du composé par leur effet stérique. Par exemple, ils restreignent la rotation libre des radicaux alkyles ou empêchent la conversion des deux conformations chaise des cycles cyclohexane l' une dans l'autre. Le radical tert-butyle volumineux reste ici de préférence en position équatoriale, car cela entraîne les interactions les plus faibles possibles avec d'autres substituants. Dans la deuxième conformation de chaise possible, le reste est en position axiale, ce qui entraîne des interactions avec d'autres substituants axiaux ( Prelog stress ). Comme ceux-ci sont énergétiquement défavorables, cet équilibre se situe fortement du côté où le groupe tert-butyle occupe une position équatoriale.
Propriétés électroniques
Les différentes positions avec lesquelles le groupe butyle se lie à la molécule entraînent des propriétés électroniques différentes qui sont causées par les effets inductifs des radicaux alkyle. Ainsi, parmi les radicaux butyle isomères, la densité électronique est la plus élevée sur le carbone tertiaire du groupe tert-butyle et la plus faible sur le groupe n- butyle. Ceci se reflète également dans l'augmentation de la basicité de la lithiés espèces de n - butyllithium via sec - butyllithium à tert - butyllithium . Le même effet est également destiné à diminuer l' acidité de l' alcool proton de l'alcool de butyle, 1-butanol , le 2-butanol et de tert - butanol responsable.
utilisation
Les lithium-alkyles sont des bases organométalliques fortes . Ils peuvent être utilisés pour la déprotonation de protons faiblement acides et pour la lithiation . Trois bases butyllithium sont disponibles dans le commerce comme réactifs standards : le n- butyllithium, le sec- butyllithium et le tert- butyllithium (augmentation de la réactivité). Le groupe tert-butyle fait partie de l'important groupe protecteur BOC .
L' agent d' hydrogénation hydrure de diisobutylaluminium (DIBAL) possède deux groupes isobutyles.
Groupes de connexion
Les groupes de substances suivants contiennent les quatre formes isomères du groupe butyle en tant qu'élément structurel :
- Butanols
- Butylamines
- Chlorobutane
- Bromobutanes
- Butylbenzènes
- Leucine (butylglycine)
- Pentanals (butyl carbaldéhydes)
- Acides pentanoïques ( acides butyl carboxyliques)
- Acétate de butyle
Preuve individuelle
- ^ Brockhaus ABC chimie. VEB FA Brockhaus Verlag, Leipzig 1965, page 46.
- ^ Hans Beyer et Wolfgang Walter : Chimie organique. S. Hirzel Verlag, Stuttgart 1984, ISBN 3-7776-0406-2 , page 792.