Couche d'ozone
La couche d'ozone est une zone de concentration accrue du gaz trace ozone (O 3 ) dans l' atmosphère terrestre , principalement dans la basse stratosphère . Il y est créé à partir de l'oxygène de l'air, car ses molécules d'O 2 sont divisées en atomes d'oxygène par la fraction la plus énergétique de la lumière solaire ( UV-C ) . Les atomes se combinent ensuite immédiatement avec un O 2 supplémentaire chacun pour former O 3 .
L'ozone lui-même est beaucoup plus sensible à la lumière que l'O 2 . Il absorbe les UV-C et UV-B et protège ainsi les plantes, les organismes, les animaux et les personnes des dommages causés par les radiations. Lorsqu'une molécule d'ozone absorbe un photon UV , il est divisé, mais dans la grande majorité des cas, l'atome d'O libéré forme immédiatement à nouveau de l'ozone. Seules les exceptions, principalement O + O 3 → 2 O 2 , signifient une perte d'ozone.
L'ozone a une grande influence sur la température de la stratosphère, d'une part par absorption UV, d'autre part, en tant que molécule inclinée, il est IR-actif et donc rayonne de la chaleur.
On considère que les physiciens français Charles Fabry et Henri Buisson ont découvert la couche d'ozone . En 1913, ils ont détecté de l'ozone dans les couches supérieures de l'atmosphère au moyen de mesures spectroscopiques UV.
Distribution mondiale
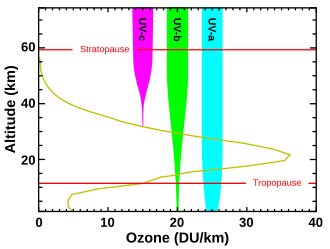
La durée de vie effective de l'ozone est suffisamment longue pour qu'il soit transporté globalement par les courants lents de la stratosphère : Bien que la majeure partie de l'ozone soit créée dans la zone de l'équateur, la majorité de l'ozone se trouve dans les latitudes modérées et élevées, aux altitudes entre 15 et 25 kilomètres. La hauteur de la colonne, mesurée en unités Dobsoniennes (UD), est comprise entre 300 et 400 DU aux latitudes modérées, et parfois plus de 500 DU aux latitudes plus élevées en début d'été, avec 100 DU correspondant à une épaisseur de 1 mm. Sous les tropiques, la couche d'ozone est élevée par l'amont de la troposphère à une altitude de 20 à 30 km et amincie à 200 à 300 UA. La hauteur de colonne la plus basse au monde dans le trou dit d' ozone , qui s'ouvre régulièrement au printemps de l'Antarctique, est parfois bien inférieure à 200 DU.
Processus
La photolyse d' une molécule d'oxygène (O 2 ) à des longueurs d'onde inférieures à 240 nm produit deux atomes d'oxygène, dont chacun se lie à une autre molécule d'oxygène, de sorte que deux molécules d'ozone sont créées :
- 3 O 2 → 2 O 3 (longueur d'onde < 240 nm)
L'ozone absorbe la lumière UV à ondes plus longues, jusqu'à environ 300 nm, les molécules d'ozone se séparant chacune d'un atome d'oxygène. Dans la grande majorité des cas, cet atome se reconnecte immédiatement à une molécule d'oxygène, de sorte que la quantité d'ozone diminue à peine :
- O 3 + O 2 → O 2 + O 3 (longueur d'onde < 300 nm)
Dans une stratosphère propre, le processus de perte le plus courant est la réaction d'un atome d'oxygène avec une molécule d'ozone. Cela crée deux molécules d'oxygène communes:
- O + O 3 → 2 O 2
C'est ce qu'on appelle le cycle ozone-oxygène , dans lequel la quantité d'ozone reste presque constante.
Observabilité
Malgré le faible nombre de molécules d'ozone à une altitude de 15 à 30 km, la couche d'ozone est perceptible dans deux phénomènes atmosphériques au crépuscule, tous deux dus à l' absorption de Chappuis :
- Immédiatement après le coucher du soleil ou avant le lever du soleil, la coloration bleue du ciel est principalement due à l'effet d'absorption de l'ozone et non - comme c'est par ailleurs le cas dans le ciel diurne - à la diffusion Rayleigh . Ce n'est qu'en 1952 que le géophysicien américain Edward Hulburt (1890-1982) reconnaît que l'absorption de Chappuis est à l'origine de cette coloration . Cette coloration particulière du ciel , connue sous le nom d' heure bleue, était déjà connue auparavant.
- Peu avant le lever du soleil ou après le coucher du soleil, l' arc d'ombre terrestre est visible. Il s'agit d'une bande bleu-gris près de l'horizon dans la position opposée au soleil. Selon une théorie controversée , sa couleur est également due à l'effet d'absorption de l'ozone.
Histoire géologique
Il y a environ 3,5 milliards d'années, l' atmosphère terrestre ne contenait pas d'oxygène libre (O 2 ). Avec l'apparition des premiers micro-organismes phototrophes à l'oxygène ( libérant de l' O 2 lors de la photosynthèse ), probablement des cyanobactéries , la libération d'oxygène (O 2 ) de l'eau a commencé. L'oxygène libéré (O 2 ) ne s'est pas initialement rendu dans l'atmosphère, mais a été consommé lors de l' oxydation des ions de métaux de base dissous dans l'eau , en particulier Fe 2+ , et du sulfure également dissous dans l'eau . Ce n'est que lorsque ces oxydations se sont terminées après une très longue période que l'oxygène libre a pu s'accumuler dans l'atmosphère terrestre. Cette phase de l' évolution de l'atmosphère terrestre est connue sous le nom de grande catastrophe de l' oxygène . L'oxygène a atteint la stratosphère par convection et diffusion, où la couche d' ozone a été créée par le cycle ozone-oxygène .
Trou dans la couche d'ozone
En tant que composant de certains gaz, en particulier les chlorofluorocarbures (CFC), le chlore et le brome pénètrent dans la stratosphère, qui contribuent alors à la dégradation de l'ozone stratosphérique. Cela augmente le rayonnement UV-B dur à la surface de la terre, ce qui a des effets négatifs sur l'homme et la nature. Dans la nuit polaire au-dessus de l'Antarctique, les nuages entrent en jeu, pour lesquels il fait autrement trop chaud dans la stratosphère sèche. Les polluants se garent sur leurs particules et sont massivement libérés au lever du soleil au printemps. Dans la partie inférieure de la stratosphère, l'ozone est presque complètement décomposé en quelques semaines. Ce n'est que lorsque le vortex polaire devient instable que les masses d'air riches en ozone pénètrent dans le trou d'ozone et le ferment, tandis que l'air pauvre en ozone pénètre parfois jusqu'en Amérique du Sud et en Australie, où il entraîne une augmentation des valeurs UV-B. Les effets sont prévisibles mais difficiles à évaluer. En 1981, Veerabhadran Ramanathan a décrit que le très fort effet de serre des seuls chlorofluorocarbures réchaufferait l' atmosphère terrestre d'un degré entier d'ici l'an 2000 si les émissions de ce gaz ne sont pas considérablement réduites.
La couche d'ozone stratosphérique n'est pas liée à l'augmentation de l'ozone qui se produit près du sol pendant le smog estival .
Scientifiques éminents dans l'étude de la couche d'ozone
- Alfred Cornu (1841-1902) a découvert que le spectre solaire s'interrompt en dessous de 300 nm.
- Carl Dorno (1865-1942), fondateur de la climatologie radiative.
- Paul Götz (1891-1954), découvreur de l' effet inverse , également connu sous le nom d' effet Götz , pour déterminer la répartition verticale de l'ozone dans l'atmosphère.
- Gordon Dobson (1889-1976) a été le premier à reconnaître les fluctuations saisonnières de l'épaisseur de la couche d'ozone.
- En 1971, Hans-Karl Paetzold (1916-2002) a souligné la menace pour la couche d'ozone des avions supersoniques civils volant à haute altitude.
- Erich Regener (1881-1955) a étudié l'équilibre oxygène-ozone dans l'atmosphère.
- Sydney Chapman (1888-1970) de lui en 1930 les relations chimiques du cycle ozone-oxygène ont été élucidés.
- Paul Crutzen (1933-2021) a reçu le prix Nobel de chimie en 1995 - avec Mario J. Molina et Frank Sherwood Rowland - "pour ses travaux sur la chimie de l'atmosphère terrestre, en particulier sur la formation et l'appauvrissement de l'ozone" .
liens web
- Chercheur : La couche d'ozone s'est stabilisée. Sur : Wissenschaft.de depuis le 31 août 2005.
- Pourquoi la couche d'ozone doit être patiente. Sur : Wissenschaft.de à partir du 15 février 2006.
Preuve individuelle
- ↑ Antje Dethof : Assimilation des données d'ozone dans le modèle ECMWF. ( Memento du 20 mai 2005 dans Internet Archive ) (PDF; 5,9 Mo), ECMWF , 2005.
- ↑ Götz Hoeppe : Himmelslicht, image miroir du climat terrestre , Université libre de Berlin
- ↑ Spencer Wear : La découverte du réchauffement climatique : autres gaz à effet de serre . Centre d'histoire de l' American Institute of Physics , aip.org