Adénine
| Formule structurelle | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
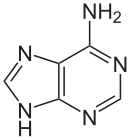
| ||||||||||||||||||||||
| Général | ||||||||||||||||||||||
| Nom de famille | Adénine | |||||||||||||||||||||
| Autres noms | ||||||||||||||||||||||
| Formule moléculaire | C 5 H 5 N 5 | |||||||||||||||||||||
| Brève description |
solide jaune clair |
|||||||||||||||||||||
| Identifiants / bases de données externes | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Information sur les médicaments | ||||||||||||||||||||||
| Code ATC | ||||||||||||||||||||||
| Propriétés | ||||||||||||||||||||||
| Masse molaire | 135,13 g mol -1 | |||||||||||||||||||||
| État physique |
fermement |
|||||||||||||||||||||
| point d'ébullition |
Décomposition à partir de 360 ° C |
|||||||||||||||||||||
| Point de sublimation |
220 ° C |
|||||||||||||||||||||
| solubilité |
pauvre en eau (0,5 g l −1 à 20 ° C) |
|||||||||||||||||||||
| consignes de sécurité | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Données toxicologiques | ||||||||||||||||||||||
| Dans la mesure du possible et selon l'usage, des unités SI sont utilisées. Sauf indication contraire, les données fournies s'appliquent aux conditions standard . | ||||||||||||||||||||||
L'adénine est l'une des quatre nucléobases de l' ADN et de l' ARN , aux côtés de la cytosine , de la guanine et de la thymine ou de l' uracile (dans l'ARN).
C'est un composé organique hétérocyclique avec un squelette purine et un groupe amino en position 6. La désoxyadénosine dans l'ADN et l' adénosine dans l'ARN sont des nucléosides qui contiennent de l'adénine. Avec la thymine ou l'uracile, il forme deux liaisons hydrogène dans l' appariement de bases Watson-Crick .
présentation
- Synthèse de Lord Todd appliquée à la formamidine et au phénylazomalononitrile .
- L'adénine peut être considérée comme un pentamère d' acide cyanhydrique et peut être préparée à partir de celui-ci dans de l' ammoniac liquide avec des rendements supérieurs à 20%.
Histoire et importance biologique
Le 12 janvier 1885, le dernier lauréat du prix Nobel, Albrecht Kossel, rapporta à la Berlin Chemical Society une découverte importante. Il a pu isoler une base riche en azote de formule empirique C 5 H 5 N 5 , pour laquelle il était dérivé du grec , à partir d'une grande quantité de pancréas bovin, qui avait été transformé par Adolph Bannow (1844-1919) dans l'usine chimique de Berlin Kahlbaum Mot «aden» pour glande suggérée par le nom adénine. Kossel a également prouvé qu'il s'agissait d'un produit de clivage de la nucléine de levure. Il a ensuite été en mesure de détecter l'adénine comme produit de clivage de l'acide nucléique.
L'adénine peut faire partie de l'ADN, de l'ARN ou de divers nucléosides et nucléotides .
Nucléosides
Via l' atome N 9 du cycle à cinq chaînons, l'adénine peut être liée de manière N- glycosidique à l' atome C 1 du ribose ; on parle alors d'un nucléoside , l' adénosine . Lorsqu'il se lie au désoxyribose , le nucléoside désoxyadénosine se forme . Contrairement à la plupart des nucléosides, la vidarabine synthétique contient de l' arabinose au lieu du ribose .
Nucléotides
L'acide phosphorique peut être lié à l' adénosine sous forme de résidu phosphate, c'est ainsi qu'il se forme
- Adénosine monophosphate (AMP)
- Adénosine monophosphate cyclique (AMPc)
- Adénosine diphosphate (ADP)
- Adénosine triphosphate (ATP)
Des molécules correspondantes se forment lorsque les résidus phosphate sont liés à la désoxyadénosine (dAMP; dADP; dATP).
L'adénosine triphosphate (ATP) joue un rôle particulier dans le métabolisme énergétique de la cellule. La réaction ATP → ADP + P libère de l' énergie , la réaction ADP + P → ATP stocke l'énergie chimiquement.
L'adénosine monophosphate cyclique (AMPc) est un deuxième messager très courant pour la transduction du signal cellulaire .
L'adénine fait également partie du nicotinamide adénine dinucléotide NAD + , qui sert de coenzyme pour le transfert d'hydrogène et est donc impliquée dans les réactions redox dans la cellule . L'adénine est utilisée pour la biosynthèse de la coenzyme S-adénosyl-méthionine , qui est utilisée dans les méthylations biologiques , par ex. B. par une Dam méthylase .
Partie d'ADN et d'ARN
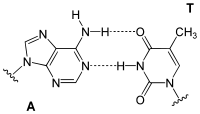
L'adénine forme deux liaisons hydrogène avec la thymidine dans la double hélice d'ADN . Lors de la transcription, en revanche, l'adénine du brin codogène d'ADN se couple avec l' uridine de l' ARNm qui vient de se former . Il existe également des appariements avec la dihydrouridine ou la pseudouridine dans l' ARNt .
|

|
|
|
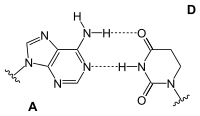
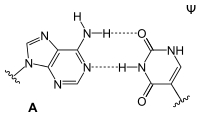
| AT paire de bases (ADN) | Paire de bases AU (ARN) | Paire de bases AD (ARN) | Une paire de bases Ψ (ARN) |
Liens connexes
|

|

|

|

|

|
| 1-méthyladénine | 2-méthyladénine | N 6 -méthyladénine | N 6 , N 6 -diméthyladénine | N 6 isopentényladénine | 2-aminopurine (isoadénine) |
liens web
- Entry for adenines in the Human Metabolome Database (HMDB) , consulté le 19 novembre 2013.
Preuve individuelle
- ↑ Entrée sur ADENINE dans la base de données CosIng de la Commission européenne, consultée le 27 mars 2020.
- ↑ adénine Fiche de données (PDF) de Carl Roth , consulté le 14 Décembre 2010.
- ↑ une entrée b sur l' adénine. Dans: Römpp Online . Georg Thieme Verlag, consulté le 12 novembre 2014.
- ↑ a b c Entrée sur l' adénine dans la base de données des substances GESTIS de l' IFA , consultée le 8 janvier 2020. (JavaScript requis)
- ↑ adénine fiche de données de Sigma-Aldrich , consulté le 16 Octobre 2016 ( PDF ).
- ^ Albert Gossauer, Structure et réactivité des biomolécules: une introduction à la chimie organique, Verlag Helvetica Chimica Acta, 2006.
- ↑ Kossel, A.: À propos d'une nouvelle base du corps de l'animal. Conférence dans: Reports of the German Chemical Society , Numéro 18, 1885, p. 79.
- ↑ Kossel, A.: Autres contributions à la chimie du noyau cellulaire. Dans: Zeitschrift für Physiologische Chemie , Volume 10, 1886, p. 248.
- ↑ Kossel, A.: À propos de la composition chimique de la cellule. Conférence dans: Archives for Anatomy and Physiology. Département de physiologie , 1891, p. 178.



